Aufgabe:
Erweiterungsaufgabe zur radikalischen Polymerisation:
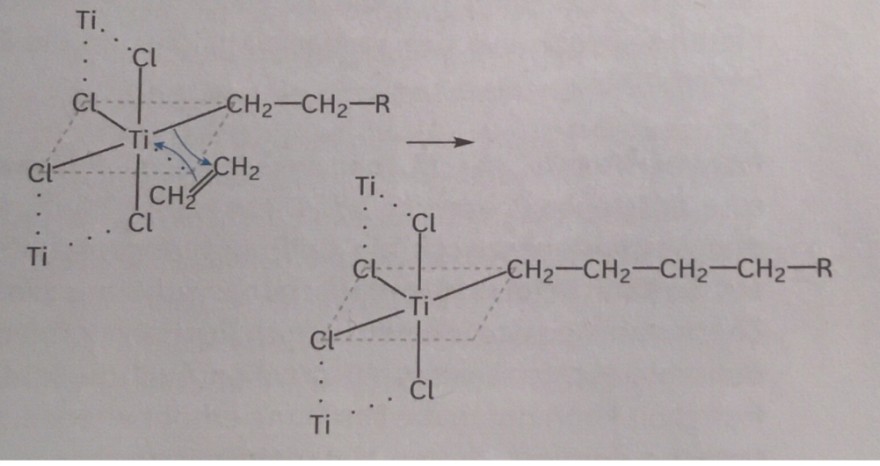
In der Abbildung unten ist die Wirkungsweise (hier TiCl4) eines Ziegler-Natta-Katalysators dargestellt, der verwendet wird, um die radikalische Polymerisation besser kontrollieren zu können und Reste zu vermeiden, sodass verlässlich unverzweigte Makromoleküle entstehen.
a) Vergleichen Sie diese Kettenwachstumsreaktion mit der geläufigen Kettenwachstumsreaktion.
Suchen Sie eine Erklärung dafür, dass diese Reaktion kontrollierter abläuft als die ohne Katalysator.
b) Machen Sie eine Vorhersage über die Unterschiede der Stoffeigenschaften eines mit und ohne Ziegler-Natta-Katalysator hergestellten Polyethen-Moleküls.
Problem/Ansatz: