Grüße chemweazle,
Welche Aussagen stimmen?
Grafik
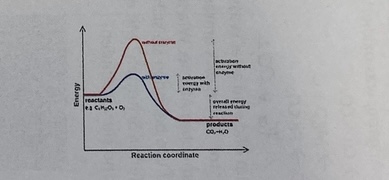
1) Auf der Grafik: sind zwei exotherme Reaktionsverläufe zu sehen.
Das stimmt. Die Produkte, Kohlendioxid und Wasser sind typisch energiearme Prdukte und sie sind energieärmer, als die Ausgangsstoffe.
In der Grafik liegen die Ausgangsstoffe(Edukte) deutlich höher in Richtung der Energie-Achse(y-Achse)(Ordinate).
2)Auf der Grafik sind zwei endotherme Reaktionsverläufe zu sehen.
Das ist falsch.
3)CO2 und H20 sind hier energiearmer als die Ausgangsstoffe.
Das ist richtig.
4) Es wird Energie frei.
Das stimmt, weil die Ausgangsstoffe energiereicher als die Produkte sind, oder anders formuliert, die Produkte sind energieärmer, als die Edukte(Ausgangsstoffe).
5)Es gibt hier keine Aktivierungsenergie.
Das ist falsch, denn die Höhe der Bergspitze der Kurven, gemessen von der Höhe der Ausgangsstoffe ist die Aktivierungsenergie.
Welche Aussagen stimmen ? 4, 3, 1