Grüße chemweazle,
f.) Wie viele Elektronen werden pro Formeleinheit Arsenik ausgetauscht?
Aufgabe:
Arsenik (As2O3) wird mit Chlorgas in wässriger Lösung zur Arsensäure (H3AsO4) und Chlorwasserstoff umgesetzt. Erstellen Sie die Stoffgleichung mit möglichst kleinen ganzzahligen Koeffizienten und beantworten Sie dann folgende Frage:
f.) Wie viele Elektronen werden pro Formeleinheit Arsenik ausgetauscht? (Geben Sie das Ergebnis als ganze arabische Zahl ab)
Reaktionsgleichung zur Oxidation von Arsenikpulver mit Chlorwasser
Redox:
As2O3(s) + 2 Cl2(aq) + 5 H2O ⇌ 2 H3AsO4 + 4 H(+)(aq) + 4 Cl(-)(aq)
Red:
Cl2 + 2 e(-) ⇌ 2 Cl(-) | mal 2
Ox:
As2O3 + 5 H2O ⇌ 2 H3AsO4 + 4 e(-) + 4 H(+) | mal 1
Was versteht man nun unter der Formeleinheit?
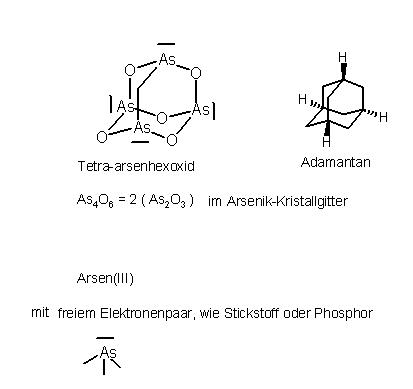
Im Kristallgitter des Arsenikminerals liegen nun As4O6-Moleküle vor. Diese enthalten jeweils 4 As-Atome.
Diese Moleküle weisen eine sog. "Hetero-Adamantan-Struktur" auf. Diese enthalten die doppelte, kleinstmögliche, stöchiometrische Formeleinheit. (s.u. und die angehängte Skizze am Ende)
Bei der Oxidation von Arsen(III) zu Arsen(V) werden pro Arsenatom 2 Elektronen abgegeben. (As(III) → As(V) + 2 e(-)
Eine Tetra-arsenhexoxid-Molekül-Einheit liefert demnach bei der Oxidation zur Arsen(V)säure 4 mal 2 Elektronen = 8 Elektronen.
Aber ich denke, der Aufgabensteller meint die kleinstmögliche Formeleinheit, de die Stöchiometrie ebenfalls wiedergibt.
As4O6 entspricht formal 2 * ( As2O3 )
Der kleinste Ausschnitt wäre dann As2O3, dieser liefert dann bei der Oxidation der As(III)-Atome zu Arsen(V)säure, isostrukturell zur Phosphorsäure, dann 2 mal 2 Elektronen = 4 Elektronen.
Arabische Zahl: 4
Skizzen