a) Phosphor steht in der 3. Periode und hat damit 2 voll besetzte innere Schalen. In der ersten Schale sind 2 Elektronen und in der 2. Schale sind 8 Elektronen.
Phosphor steht in der 5. Hauptgruppe und hat demnach 5 Elektronen auf der äußeren Schale.
b)
Calcium | 4. Periode und 2. Hauptgruppe
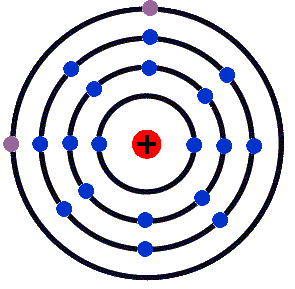
c)
Die Elemente einer Periode von Links nach rechts sind nach der Ladungszahl des Atomkerns geordnet. Und damit auch nach der Anzahl der Elektronen in der äußeren Schale.
d)
Chemisch verwandte Elemente findet man in einer Hauptgruppe. Also in einer Spalte untereinander. Alle diese Elemente haben gleich viele Elektronen in der äußeren Schale. Außnahme ist das Helium mit 2 statt 8 Elektronen in der äußeren Schale.