Hi, hier chemweazle,
Lässt sich das Bromwasser irgendwie dort mit einbringen, wenn ja wie?
Ja, zum Schluß ergänzend zur Bayer-Probe, ebenfalls ein Hinweis auf auf die Doppelbindung
Zum Schluß einige Tropfen vom Rohprodukt(Alken) zu einigen ml Bromwasser geben. Es findet dann die Entfärbung bedingt durch die Addition der braunen Brommoleküle an die C-C-Doppelbindungen zu farblosem Dibromalkan statt.
Die Entfärbung des Bromwassers ist ein nicht immer eindeutiger Hinweis auf das Vorhandensein einer C-C-Doppelbindung bzw. C-C-Dreifachbindung.
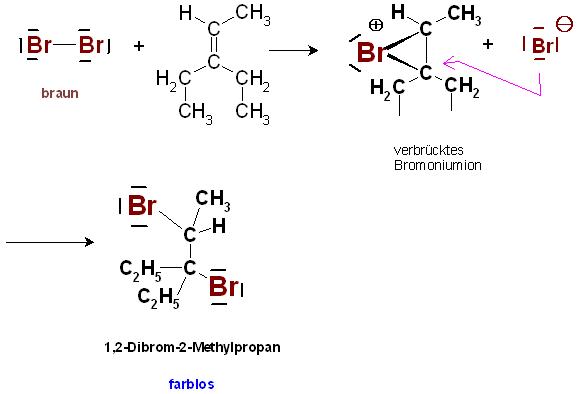
Hierbei werden die braun gefärbten Brommoleküle an die C-C-Doppel- oder C-C-Dreifachbindung addiert. Dabei enstehen farblose Dibromalkanverbindungen.
Die Bromaddition verläuft, wie alle sonstigen Halogenadditionen an Doppelbindungen über das Zwischenprodukt Haloniumion(Bromoniumion).
Skizze
Reaktionsmechanismus erstellen
Klausuraufgabe:
3 Ethyl- 3 pentanol wird mit Schwefelsäure versetzt und erhitzt, Produkt wird mit der Bayer-Probe und mit Bromwasser auf das Vorhandensein der Doppelbindung getestet.
Mein Ansatz war eine Eliminierung, bei der die Schwefelsäure ein H+ an die OH Gruppe abgibt, damit sich diese besser abspaltet. Das entstehende HSO4- greift ein Wasserstoff als Base an, sodass eine Doppelbindung entstehen kann. Das Produkt wird dann mit der Bayer Probe getestet, welche sich entfärbt.
Genau, Richtig E1-Reaktion
Also das Hydrogensulfation ist eine ganz schwache Base, denn die Schwefelsäure ist in 1 molarer Lösung vollständig dissoziiert. Das Hydrogensulfation schafft es nicht, wegen der schwachen Basizität, ein Proton auch von einem Carbeniumion, abzuspalten.
Es ist sicherlich die monomolekulare Eliminierung (E1-Reaktion). Der Alkohol wird am Elektronenpaar der OH-Gruppe protoniert, es bildet sich das Alkyloxoniumion. Diese Protonierung ist ein sehr sehr schneller Schritt wie alle Protonenübertragungen. Dann folgt der langsamste Schritt, der geschwindigkeitsbestimmende Schritt, die Abspaltung des Wassers aus dem Alkyloxoniumion unter der Bildung des Carbeniumions.
Dieser Wasserabspaltungsschritt ist eine sehr langsame Reaktion, diese läuft nur an einer Sorte Teilchen, dem Oxoniumion, das ist der protonierte Alkohol, ab. Also die Molekularität ist somit 1, monomolekulare, unimolekulare Reaktion. Eine Sorte Teilchen ist auch im Übergangszustand beteiligt.
Protonierung des Alkohols zum Alkyloxoniumion
( CH3-CH2)3C—OH + H(+)(aq) ⇌ ( CH3-CH2)3C—OH2(+)
Langsamster , Geschwindigkeitsbestimmender Schritt, die Wasserabspaltung, Eine Sorte Teilchen im Übergangszustand
| ( CH3-CH2)3C—OH2(+) | ⇌ | [ ( CH3-CH2)3C····OH2(+) ](≠) | ⇌ | ( CH3-CH2)3C(+) | + | H2O |
| Oxoniumion | ⇌ | Übergangszustand | ⇌ | Carbeniumion | | |
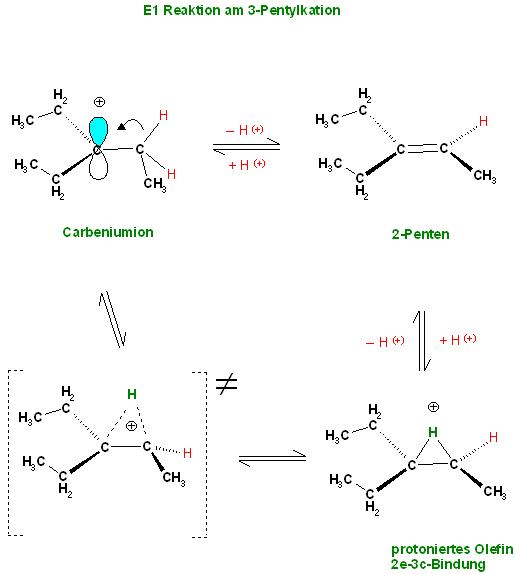
Olefinbildung aus dem Carbeniumion
Beim Carbeniumion klappt ein Elektronenpaar einer benachbarten C-H-Bindung zum postiv geladenen C-Atom hin. Von dem Elektronenpaar, welches zum positiven C-Atom klappte springt das vormals gebunndene Proton des H-Atom weg in die Lösung. Nun ist das Alken(Olefin) enstanden.
Skizze
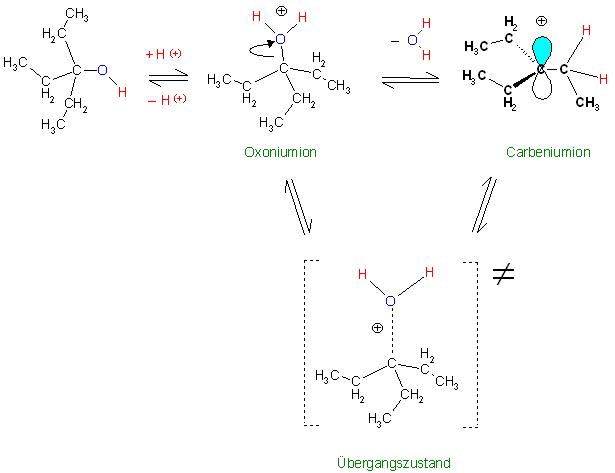
Skizze