Hi, hier chemweazle,
Hydrierung von Ölsäure, cis-octadec-9-ensäure
Hydrierung von ölsäure mit elementaren Wasserstoff. Dabei entsteht Wasser und ein fettalkohol
Ich weiß nicht wie ich die Reaktionsgleichung aufstellen soll und was für ein fettAlkohol entstehtden?
Die Ölsäure ist eine einfach ungesättigte Carbonsäure, d.h. sie besitzt eine einzige Doppelbindung und die Carboxylgruppe als funktionelle Gruppen. Das sind 2 funktionelle Gruppen.
Das einfachste Beispiel einer ungesättigten( einfach ungesättigten ) Carbonsäure ist die Acrylsäure.
2HC=CH-CO2H
Es handelt sich um eine Alkensäure mit 18 C-Atomen. Also eine Octadecensäure. Die C-C-Doppelbindung fängt am 9ten C-Atom an und endet am 10ten C-Atom, wenn man nach der moderneren Zählweise die Carboxylgruppe mit 1 nummeriert.
Octadec-9-en-säure
CH3-( CH2 )7-CH=CH-( CH2 )7-CO2H
Eine Möglichkeit zur Abkürzung wäre:
C8H17-CH=CH-( CH2 )7-CO2H
Zur Frage welcher primäre Alkohol entsteht:
Das Skelett der einfach ungesättigten Fettsäure hat 18 C-Atome.
Addiert man 2 H-Atome oder 1 H2-Molekül an die C-C-Doppelbindung so entsteht eine gesättigte Fettsäure mit 18 C-Atomen, es ist die Octadecansäure mit dem Trivialnamen Stearinsäure.
Hier wird einfach ein Alken zum Alkan reduziert, indem 2 H-Atome an die Doppelbindung addiert werden.
CH3-( CH2 )7-CH=CH-( CH2 )7-(C=O)OH + H2 ⇌ CH3-( CH2 )7-CH2-CH2-( CH2 )7-(C=O)-OH
Wird die Carboxylgruppe, ((C=O)-OH) zur prim. Alkoholgruppe, (CH2-OH) reduziert, so entseht ein prim. Alkohol mit 18 C-Atomen, also der Octadecanol. ( Octadeca, octa =8, deca =10, octadeca = 8 + 10 =18 )
1-Octadecanol, Trivialname: Stearylalkohol
CH3-( CH2 )7-CH2-CH2-( CH2 )7-CH2-OH
CH3-( CH2 )16-CH2-OH
C18H37-OH
Die Wasserstoffaddition an C-C-Doppelbindungen und C-C-Dreifachbindungen, C-N-Doppelbindungen und C-N-Dreifachbindungen gelingt mit den geläufigen Platinmetallen und Nickelmetall als Hydrierungs-Katalysatoren.
Mit einigen speziellen Katalysatoren, diese bestehen aus Rhenium, Cobalt, Kupfer, lassen sich bei hohen Temperaturen im Bereich von 100°C bis 300 °C und sehr hohen Drücken zwischen 100 bis 330 bar Carbonsäuren zu prim. Alkoholen unter Wasserabspaltung hydrieren.
R-(C=O)-OH + 2 H2 ⇌ R-(CH2)-OH + H2O
Für die Reduktion einer Carboxylgruppe mit elementaren Wasserstoff zur prim. Alkoholgruppe( CH2-OH) werden insgesamt 4 Wasserstoffatome bzw. 2 Wasserstoffmoleküle verbraucht.
Einmal wird formal der doppelt gebundene Sauerstoff der Carboxylgruppe durch 2 H-Atome ersetzt und das O-Atom, in der Gleichung blau hervorgehoben, benötigt noch 2 H-Atome für die Wasserbildung.
Zur Frage wieviel mol Wasserstoff werden für die Reduktion von 1 mol einfach ungesättigte Carbonsäure zu 1 mol gesättigten, dh. ohne Doppelbindungen, primären Alkohol benötigt.
1 H2 für die C-C-Doppelbindung, 2 H2 für die Carboxylgruppe
Bzw.1 mol H2 für 1 mol C-C-Doppelbindungen, 2 mol H2 für 1 mol
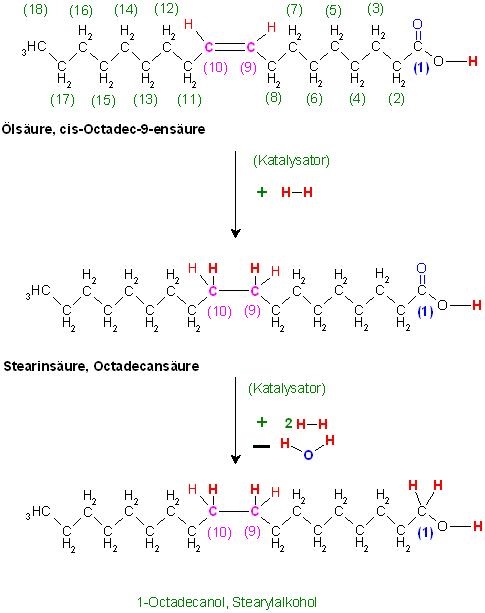
Reaktionsgleichung
CH3-( CH2 )7-CH=CH-( CH2 )7-(C=O)OH + 3 H2 ⇌ CH3-( CH2 )7-CH2-CH2-( CH2 )7-(CH2)-OH + H2O