Hi, hier chemweazle,
Zu
Wie kann ich W deuten kann?
Zusammenhang zwischen innerer Energie, Reaktionswärme bei konstantem Druck und Volumenarbeit:
Beispiel: Reaktion von Zink mit Salzsäure ( exotherm, Volumen vergrößernd)
Ich verstehe bei dieser Aufgabe nicht ganz wie ich W deuten kann? Ich glaube ich kann die Abbildung nicht deuten. Wie kommt es das Qp und W nach unten beide zeigen? 764A735B-6499-45CB-B4EF-0C4B939F5E68.jpeg
Reaktionsgleichung
Zn0(s) + 2 HCl(aq) → ZnCl2(aq) + H2(g) ↑
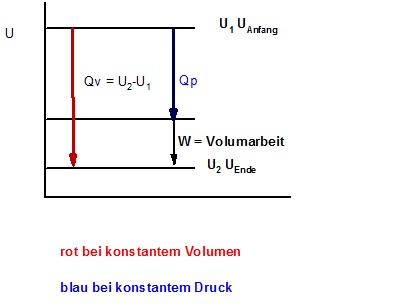
W ist die Volumenausdehnungsarbeit gegen den Atmosphärendruck, allgemein Volumarbeit genannt, des enstehenden Gases (Wasserstoff).
Fall A, isochore Reaktionsführung, bei konstantem Volumen, ohne Volumarbeit
Würde die Reaktion in einem druckfesten Autoklaven bei konstantem Volumen durchgeführt, so würde die gesamte Reaktionsenergie U2 - U1 in Form von Wärme an die Umgebung abgegeben.
Δ U = U2 - U1 = Qv
Fall B, isobare Reaktionsführung, bei konstantem Druck, mit Volumarbeit
Würde die Reaktion in einem Gefäß ohne Deckel, oder mit undichtem Deckel oder mit einem verschiebbaren Deckel, durchgeführt, so wird ein Teil der Reaktionsenergie in Form von Volumarbeit, w, und dafür weniger Wärme an die Umgebung abgegeben, als es bei konstantem Volumen der Fall ist.
Δ U = U2 - U1 = Qp + w
Die bei konst. Druck an die Umgebung abgegebene Wärme im Fall B ist kleiner, geringer, als die an die Umgebung abgegebene Wärme bei Fall A, weil ein Teil der freiwerdenden Reaktionsenergie in Form von Volumarbeit gegen den Atmossphärendruck verrichtet wird.
Qp < Qv
Skizze