Die anderen Aufgaben habe ich alle gelöst, nur bei diesen Beiden blicke ich leider nicht durch. Wäre über Hilfe sehr dankbar.
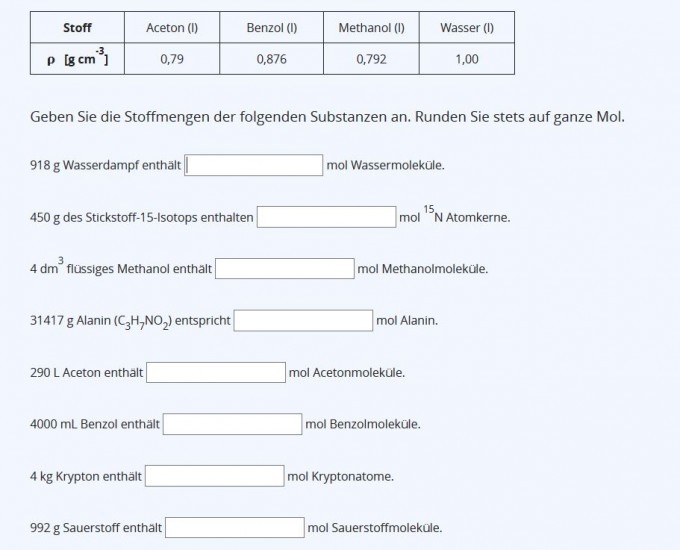
4 dm3 flüssiges Methanol enthält ___________ mol Methanmoleküle.
450 g des Stickstoff-15-Isotops enthalten ____________ mol 15N Atomkerne.